NEN Medikamentöse Therapie
Operative Therapie neuroendokriner Tumore:
Operatives Vorgehen beim neuroendokrinen Tumoren Des Dünn- oder Dickdarms
Die Therapie der neuroendokrinen Tumore kann in kurative (="heilende") und palliative ("symptomlindernde") Eingriffe unterteilt werden. Kurative Eingriffe sind insbesondere die Entfernung von Dünndarm-NET und Appendix-NET, wenn keine Lebermetastasen vorliegen. Hier werden in den meisten Fällen Entfernungen von Dünndarmteilen, z.T. mit dem rechtsseitigen Dickdarm (Hemikolektomie rechts) durchgeführt.
Palliative Eingriffe, z.B. die Reduktion von Tumormasse bei ausgeprägtem Karzinoid-Syndrom und insbesondere die Entfernung des Primärtumores, bringen für den Patienten auch bei ausgedehnter Metastasierung, z.B. in der Leber, oft einen Zuwachs an Wohlbefinden. Zudem werden Komplikationen, die durch das ungehinderte Wachstum des Primärtumors hervorgerufen werden, verhindert. Hier ist besonders der tumorbedingte Darmverschluss (Ileus), Darmblutungen oder Einwachsen des Tumors in lebenswichtige Organe oder Blutgefäße, zu nennen.
Die Behandlung der meist in der Leber gelegenen Metastasen ist auch hier vielfältig und reicht von der chirurgischen Entfernung von großen Teilen der Leber bis zur lokalen Abtragung durch Hitze (Radiofrequenzablation), Kälte (Kryoablation) oder über einen Verschluss der zuführenden Gefäße mit Chemotherapeutika über ein Kathetersystem (transarterielle Chemoembolisation), welches zumeist durch die Leiste eingebracht wird.
Nach biochemischer Sicherung des Insulinoms ist die Operationsindikation immer gegeben. Die einzig kurative Behandlungsmethode eines Insulinoms ist die komplette operative Entfernung. Hierdurch werden die Symptome dauerhaft beseitigt. Angestrebtes Verfahren bei gutartigen Insulinomen ist die Enukleation (Ausschälung) des Tumors.
Eine operative Behandlung von Gastrinomen ist immer angezeigt, auch bei negativem Nachweis der bildgebenden Verfahren, wenn keine diffusen Lebermetastasen vorliegen. Standardtherapie ist die Eröffnung des Zwölfingerdarmes (Duodenum) und Resektion von Duodenalwandgastrinomen sowie die Enukleation von pankreatischen Gastrinomen im Kopf oder die Linksresektion bei Tumoren im Korpus-Schwanz-Bereich. Abgesehen von der Resektion/Enukleation des Primärtumors ist eine ausgedehnte Lymphknotenentfernung um den Zwölffingerdarm, die Bauschspeicheldrüse und der Leber notwendig.
VIPome und Glukagonome sollten ebenfalls einem aggressiven chirurgischen Vorgehen unterzogen werden.
Die chirurgische Therapie spielt unter den Optionen bei NFPT die entscheidende Rolle. Das Hauptziel ist die komplette Entfernung des Tumors und seiner Metastasen, da dies die einzige Heilungschance für die Patienten darstellt, Symptome lindert und die Überlebensrate steigert.
Kleine NFPT ohne Hinweise auf Metastasierung sollten parenchymsparend entfernt werden. Bei größeren NFPT im Bereich des Pankreaskopfes sollte dagegen immer eine partielle Pankreatikoduodenektomie (sog. Whipple'sche Operation) durchgeführt werden. Hierbei ist inzwischen die pyloruserhaltende Variante die Methode der Wahl. Bei Tumoren des Schwanzes der Bauchspeichedrüse wird der tumortragende Abschnitt der Bauchspeicheldrüse mit Milz und Lymphknoten entfernt.
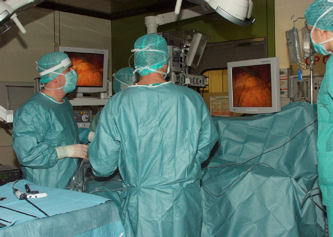
Laparoskopische Chirurgie für kleine NPTs ist sinnvoll, technisch machbar und sicher. Die Planung und Durchführung sollte allerdings nur in Zentren erfolgen, die eine ausgewiesene Expertise für die endokrine Pankreaschirurgie und die laparoskopische Chirurgie im Allgemeinen haben. Unsere Klinik führt bereits seit mehreren Jahren laparoskopische Operationen bei NPTs erfolgreich durch.
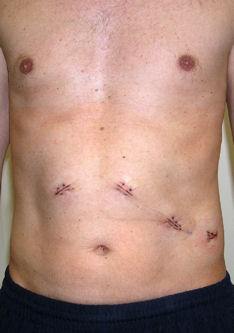
Die laparoskopische Enukleation sollte für benigne unter 2cm durchmessende Tumoren reserviert sein. Dies gilt insbesondere für Insulinome, aber auch kleine NFPT. NPTs im Pankreaskopf können enukleiert im Pankreaskorpus oder -schwanz durch Enukleation oder Pankreaslinksresektion behandelt werden.
Interventionelle Therapien:
Lokal-ablative und loko-regionäre Therapieverfahren
Einleitung
Im Rahmen einer fortschreitenden Tumorerkrankung kommt es zur Absiedlung von Tumorzellen (Metastasen) in weitere Gewebe. Oftmals sind es zuerst Lymphknotenmetastasen in der Umgebung des Primärtumors. Danach streuen die Tumorzellen bei bösartigen Neubildungen des Magen-Darm-Traktes (gastrointestinal) sowie der Bauchspeicheldrüse (Pankreas) über die ableitenden Venen und die Pfortader in die Leber. Dort werden die Tumorzellen, aufgrund der besonderen Anatomie der Leber, gefiltert und es entstehen Lebermetastasen. Insgesamt ist die Leber der häufigste Fernmetastasierungsort bei Patienten mit neuroendokrinen Tumoren (NET) des gastro-entero-pankreatischen Systems. Lebermetastasen können solitär (einzeln), multipel (mehrere, zählbar) oder disseminiert (diffus, nicht mehr zählbar) auftreten. Es bestehen verschiedene Ansätze Lebermetastasen zu therapieren. Neben herkömmlichen Therapien wie Operation oder Chemotherapie, gibt es leberspezifische Verfahren, die Tumorlast bei NETs zu verringern. Dazu zählen verschiedene loko-regionäre Verfahren, welche im Folgenden erläutert werden.
Lokal-ablative Verfahren
Die bildgesteuerte perkutane Radiofrequenzablation (RFA) ist die am weitesten verbreitete und am besten evaluierte lokal-ablative Methode. Dabei wird über einen Zugang durch die Haut (perkutan) gezielt Tumorgewebe mit einer Sonde erhitzt und damit zerstört. Allerdings sind nicht alle Lebermetastasen für eine RFA geeignet. Hierbei spielen die Zahl und die Größe der Metastasen, genauso wie die Tumorbiologie und die Erfahrung des Therapeuten eine wichtige Rolle. Die RFA kann zusammen mit der Operation einen potentiell kurativen (auf Heilung zielenden) Ansatz darstellen oder dazu beitragen, möglichst viel Tumorgewebe in der Leber zu zerstören. Dabei kann die RFA wiederholt angewendet werden und ist mit einer niedrigen Komplikationsrate behaftet. Als Alternativen zur RFA stehen u.a. die Mikrowellenablation oder perkutane Kryotherapie zur Verfügung.
Loko-regionäre Verfahren - Transarterielle Embolisation und Chemoembolisation
Lebermetastasen von NET (siehe Abb. 1) sind sehr gut durchblutet und werden zu >90% von der Leberarterie versorgt (siehe Abb. 2). Das umgebende gesunde Lebergewebe hingegen bezieht nur ca. 20% seiner Blutversorgung aus der Leberarterie und zu ca. 80% aus der Pfortader (V. portae). Diese tumor-spezifischen Eigenschaften werden sich in den transarteriellen Therapieformen wie z.B. der selektiven hepatischen transarteriellen Embolisation (TAE) oder transarteriellen Chemoembolisation (TACE) zunutze gemacht.
Dazu wird unter örtlicher Betäubung die Leistenarterie punktiert und darüber ein Katheter in die Leberarterie vorgeschoben. Zuerst wird mit Kontrastmittel unter Röntgen-Durchleuchtung die Durchblutung der Lebermetastasen dargestellt (siehe Abb. 2). Danach kann die Arterie, die den Tumor in der Leber versorgt gezielt verschlossen (embolisiert) werden, unter Verwendung diverser Partikel. Die selektive Embolisation (TAE) führt zu einer gezielten Minderdurchblutung (Ischämie) des Tumorgewebes.
Die TACE (transarterielle Chemoembolisation) beruht auf den gleichen Überlegungen wie die TAE und ist dieser ähnlich. Allerdings wird bei der TACE zusätzlich selektiv ein Chemotherapeutikum in die tumor-versorgende Arterie gegeben. Dadurch kann eine sehr hohe Konzentration des Chemotherapeutikums in dem Tumorgewebe erreicht werden. Zusätzlich erreicht man eine Wirkungsverstärkung der Chemotherapie durch die anschließende Embolisation des Gefäßes. Mittlerweile stehen moderne Partikel zur Verfügung, die das Chemotherapeutikum gezielt im Tumor freisetzen ("drug eluting beads"; DEB).
Beide Verfahren (TAE und TACE) werden angewendet um die Tumorlast in der Leber zu verringern oder um bei funktionellen NETs die Beschwerden, bedingt durch die Hormonausschüttung, zu lindern.
Loko-regionäre Verfahren -Radioembolisation
Die selektive intraarterielle Radiotherapie (Radioembolisation) nutzt den transarteriellen Zugang zu den Tumorgefäßen um eine gezielte Strahlentherapie durchzuführen. Dazu werden Harz- oder Glas-Partikel an die ein radioaktives Element (z.B. Yttrium) gekoppelt ist gezielt in die Leber appliziert. Wie bei der TAE/TACE beruht das Prinzip der lokalen intraarteriellen Radiatio (Strahlung) auf der Tatsache, dass die Lebermetastasen überwiegend über die Leberarterie, das gesunde Lebegewebe hingegen überwiegend über die Pfortader versorgt werden. Auch hier wird über einen Zugang in der Leiste die Leberarterie aufgesucht. Zusätzlich zur TAE/TACE werden Umgehungskreislaufe während dieser Behandlung unterbunden. Nach einem ersten Testlauf zur Überprüfung der möglichen Verteilung der radioaktiven Partikel in der Leber, erfolgt in einer zweiten Sitzung die Behandlung der Lebermetastasen. Während das gesunde Lebergewebe weitestgehend geschont wird, erfolgt durch die Radioembolisation eine Bestrahlung des Tumors mit sehr hohen Dosen, wie sie durch eine klassische Strahlentherapie nicht erreicht werden können.
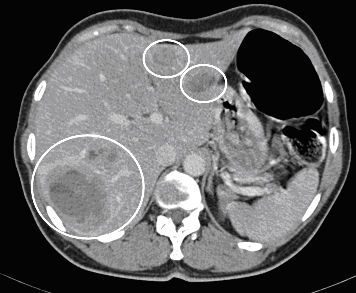
Abb. 1:
Computertomographie (CT) mit Kontrastmittel (KM) und Darstellung mehrerer metastasensuspekten Leberläsionen (weiße Ringe). Dieses CT wurde ebenfalls verwendet zur Planung einer TACE in Abhängigkeit von der Lokalisation der Metastasen.
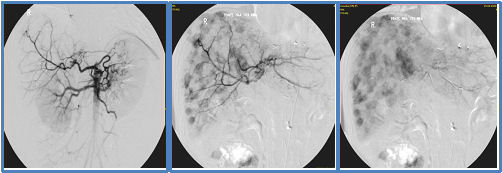
Abb. 2:
Angiographie mit Darstellung der Gefäßabgänge der Bauch-Aorta (A) und selektiver Kontrastierung der Leberarterie (B) mit Hervortreten der diffusen Lebermetastasen (B,C).
Endoskopie:
Wir führen routinemäßig interventionelle Eingriffe am Gallengangssystem und Pankreas wie Stentimplantationen und Zystendrainagen mit großer Expertise durch.
Aufgrund der langjährigen Betreuung von NET Patienten haben wir auch große Erfahrung in der lokalen Abtragung lokalisierter kleiner NETs im Gastrointestinaltrakt.Zur endoskopischen Ultraschalldagnostik incl. Punktionen stehen moderne leistungsfähige Endosonographiegeräte zur Verfügung.
Biotherapie:
Die sogenannte Biotherapie mit Somatostatinanaloga ist häufig die erste Therapie, die bei Patienten mit neuroendokrinen Tumoren eingesetzt wird. Sie beruht auf dem Vorhandensein von Somatostatinrezeptoren (Andockstationen für Somatostatin) auf der Tumorzelle. Die Wirkung dieser Medikamente ist zweifach. Bei den funktionell aktiven Tumoren, die Hormone wie z.B. Serotonin produzieren, wird die Sekretion der Hormone vermindert. Dadurch können Beschwerden, die auf Hormonsekretion beruhen, wie Flush oder Durchfälle deutlich gebessert werden. Darüber hinaus konnte kürzlich eine Studie (PROMID Studie), die unter Federführung des Marburger NET-Teams bei Patienten mit NENs des Dünndarms durchgeführt wurde, zeigen, dass diese Medikamente auch antiproliferativ wirksam sind, das heißt das Tumorwachstum aktiv bremsen können. Bei mit Octreotid-LAR behandelten Dünndarm-NEN-Patienten waren im Verlauf 67% der Patienten stabil gegenüber nur 37% der mit Placebo behandelten Patienten. Es gibt in dieser Substanzgruppe aktuell zwei zugelassene Medikamente: Octreotid (Sandostatin®) und Lanreotid (Somatuline®). Ein weiterer Wirkstoff (Pasireotid) befindet sich in klinischer Prüfung. Octreotid und Lanreotid sind meist sehr gut verträglich. Gelegentlich kommt es zu leichten Nebenwirkungen wie Durchfall, Blähungen oder der Bildung von Gallensteinen. Um die Verträglichkeit zu testen, kann Octreotid zunächst 3x/d unter die Haut gespritzt werden. Ist die Verträglichkeit gut, wird die Therapie mit Monatsdepotpräparaten intramuskulär (Octrotid-LAR) oder subkutan (Lanreotid-Autogel) durchgeführt. Insbesondere bei langsam wachsenden NEN des Dünndarms ist die Biotherapie häufig langfristig als Monotherapie erfolgreich. Interferon ? wurde erfolgreich in der Therapie der midgut-NENs eingesetzt und wirkt sowohl antisekretorisch als auch antiproliferativ, hat aber in den letzten Jahren aufgrund der doch häufigen Nebenwirkungen im Vergleich zu anderen Therapieoptionen an Bedeutung verloren, kann aber im Einzelfall durchaus eine Therapiemöglichkeit beim Dünndarm-NEN darstellen.
Chemotherapie
Eine Chemotherapie wird erfolgreich bei folgenden zwei Untergruppen von NEN eingesetzt: Dies sind einmal die neuroendokrinen Karzinome (NEC), bei denen es sich um eine sehr schnell wachsende Unterform der NEN handelt, die sich biologisch eher wie kleinzellige Bronchialtumore verhalten. Hier wird klassischerweise eine Therapie aus einem platinhaltigen Wirkstoff (Cisplatin oder Carboplatin) mit Etoposid angewandt. In den meisten Fällen sprechen die NEC primär gut an, rezidivieren aber nach Therapieende/-pause häufig schnell. Als Zweitlinientherapie werden z.B. Temozolomid und Capecitabine oder Irinotecan-haltige Schemata eingesetzt. Bei den gut differenzierten NENs spielt die Chemotherapie nur bei Tumoren, deren Ursprung im Vorderdarm zu finden ist, wie Pankreas, Bronchus und Magen, eine Rolle. Seit langem werden bei diesen Tumoren intravenöse Chemotherapien mit Streptozotocin (Nebenwirkungen: nephrotoxisch (nierenschädigend), Übelkeit, Erbrechen, leichte Blutbildveränderungen) in Kombination mit 5-FU oder Doxorubicin angewandt, die meistens recht gut verträglich sind. Eine Therapiealternative stellt Dacarbazin (Nebenwirkungen: leichte Blutbildveränderungen, Übelkeit, Erhöhungen der Leberwerte) dar, das einmal im Monat infundiert wird und ein günstiges Nebenwirkungsprofil hat. Eine dem Darcabazin verwandte Substanz, die als Tablette gegeben wird, ist Temozolomid (Temodal®). Mit all diesen Chemotherapien kann bei ca. zwei Drittel der Patienten eine Stabilisierung der Erkrankung (partielle Remission oder stable disease) erreicht werden. Bei allen Chemotherapien achten wir auf eine optimale begleitende Therapie, so dass die Nebenwirkungen möglichst gering sind. Bei den NEN des midguts, also den klassischen NEN des Dünndarms, spielt die Chemotherapie keine Rolle, da diese weitgehend chemoresistent sind und die Ansprechraten nur gering sind.
Molekular zielgerichtete Therapie:
In den letzten Jahren sind mit Everolimus und Sunitinib zwei Substanzen zugelassen worden, die zielgerichtet bestimmte intrazelluläre Mechanismen in der Tumorzelle blockieren. Beide Substanzen sind als Tabletten verfügbar. Bei Everolimus (Afinitor®) handelt es sich um einen sogenannten mTor-Inhibitor, bei Sunitinib (Sutent®) um einen Tyrosinkinaseinhibitor. Beide Substanzen wurden in randomisierten doppelblinden Studien geprüft und sind zurzeit die Medikamente, für die die beste Evidenz (d.h. Wirksamkeitsnachweis) vorliegt. Bei progredienten (also wachsenden) NEN führen diese Substanzen zu einer Verdopplung des progressionsfreien Überlebens (der Zeit, in der der Tumor nicht wächst). Beide Substanzen sind aktuell nur zur Therapie von NEN des Pankreas zugelassen. Für Everolimus gibt es auch Hinweise auf eine Wirksamkeit bei Dünndarm-NEN. Es ist jedoch dafür nicht zugelassen und muss ggf. bei der Krankenkasse beantragt werden. Die orale Therapieform als Tablette ist bei beiden Substanzen attraktiv, es gibt jedoch nicht selten Nebenwirkungen. Bei Everolimus können typischerweise Blutbildveränderungen, Verstärkung eines vorbestehenden Bluthochdrucks oder Diabetes, Diarrhoe, Aphthen (offene Stellen im Mund) und Pneumonitis (Veränderungen des Lungengewebes) auftreten. Bei Sunitinib kommen neben Blutbildveränderungen Appetitlosigkeit, gastrointestinale Nebenwirkungen, erhöhter Blutdruck und ausgeprägte Müdigkeit (Fatigue) sowie selten das Hand-Fuß-Syndrom, Geschmacksstörungen und Haarverfärbungen vor.
Nuklearmedizinische Therapie neuroendokriner Neoplasien:
Peptidrezeptor-Radio-Therapie (PRRT)
Wie im Bereich der Diagnostik ist es auch bei der Therapie oberstes Ziel möglichst viel radioaktiven Stoff (Radiopeptid oder auch Radioligand genannt) in die Zellen zu schleusen und von dort wirken zu lassen.
Ist der radioaktive Stoff ein überwiegend Gamma-Strahlen aussendender Stoff wie z.B. 111Indium, so ist er für Diagnostik gut geeignet. Handelt es sich hingegen um überwiegende Beta--Strahler wie 90Yttrium oder 177Lutetium, so sind diese für Therapie-Zwecke günstig.
Grundlage der am meisten verwendeten Radioliganden ist der Stoff DOTATOC oder DOTATATE. Man hat mehrer radioaktive Strahler zur Auswahl, die in den sogenannten Chelator DOTA eingebunden werden. Üblich ist heute die Therapie mit 90Yttrium oder 177Lutetium.
Vorraussetzungen
Vorraussetzung zur Durchführung der Therapie ist, dass mehrere Orte eines Organs (zum Beispiel Leber) oder mehrer Organe betroffen sind, denn bei einzelnen Herden ist die Operation die Methode der Wahl. Letztlich kann nur die Operation NEN-Erkrankungen vollständig und dauerhaft heilen. Einige weitere Vorraussetzungen das Labor betreffend sind ebenfalls zu klären, um Nebenwirkungen an Nieren oder Blutbild zu vermeiden. Die Nieren werden während der Therapie in jedem Fall zusätzlich durch eine Aminosäure-Lösung geschützt.
Grundvorrausetzung vor jeglicher Therapie mit DOTATOC/DOTATATE ist in jedem Fall, dass der Tumor den Stoff DOTATOC/DOTATATE kräftig anreichert, was durch eine Szintigraphie im Vorfeld untersucht wird.
Wirksamkeit der Radioliganden-Therapie
Bezüglich der Wirksamkeit der Therapie liegen diverse, europäische Studien vor. Zusammenfassend lässt sich sagen, dass deutliche Rückbildungen um mehr als 50% des Volumens bei ca. 20% der Therapien zu erwarten sind, geringere Rückbildungen (Tumorrückbildung < 49% und > 25%) sind in ca. 10-20% der Fälle nachweisbar, während stabiles Tumorverhalten (SD) in gut 50% das häufigste Ergebnis ist und als Therapie-Erfolg angesehen werden kann.

